📍 P.life Papers | July 2025
Exercise after chemotherapy for colon cancer
🎙️ Based on the podcast episode “Exercise as Treatment”
📚 Source: Courneya et al., NEJM 2025 – DOI: 10.1056/NEJMoa2502760
Introduction
Exercise after chemotherapy for colon cancer.
Colorectal cancer ranks as the third most common cancer and the second leading cause of cancer-related death globally. Despite advances in surgery and adjuvant chemotherapy, many patients still face a high risk of recurrence — especially those with stage III or high-risk stage II colon cancer.
But what if a simple, low-cost, and widely accessible tool could significantly improve survival outcomes?
That’s exactly what the CHALLENGE Trial, a phase 3 randomized study published in the New England Journal of Medicine, set out to investigate. The results are compelling.
🎯 Study Objective
The CHALLENGE Trial aimed to determine whether a structured, three-year exercise program, initiated shortly after completion of adjuvant chemotherapy, could improve disease-free survival (DFS) in patients with resected colon cancer.
🧪 Study Design
- Population: 889 patients with stage III or high-risk stage II colon adenocarcinoma.
- Randomization: 1:1 to structured exercise vs. health education only.
- Intervention:
- Exercise Group: Behavioral support + goal of ≥10 MET-hours/week.
- Control Group: General health education materials only.
- Follow-up: Median of 7.9 years.
- Primary Endpoint: Disease-free survival (DFS).
- Secondary Endpoints: Overall survival (OS), physical function (self-reported and objective), cardiorespiratory fitness.
📈 Key Results
Exercise after chemotherapy for colon cancer
✅ Disease-Free Survival (DFS)
- Hazard Ratio: 0.72 (95% CI: 0.55–0.94; p = 0.02)
- 5-Year DFS:
- Exercise Group: 80.3%
- Control Group: 73.9%
- 📊 Absolute difference: +6.4 percentage points
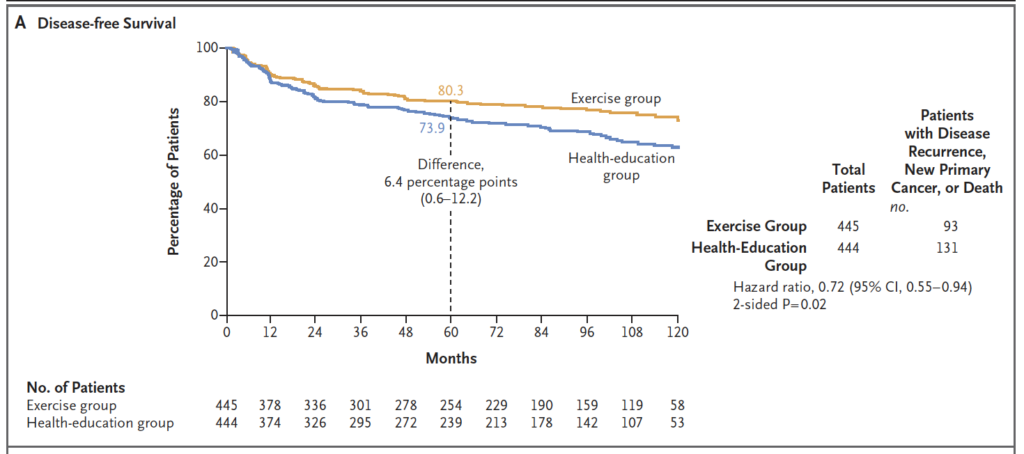
DFS
Survival curves began to separate after 1 year and continued to diverge over the long term.
✅ Overall Survival (OS)
- Hazard Ratio: 0.63 (95% CI: 0.43–0.94)
- 8-Year OS:
- Exercise Group: 90.3%
- Control Group: 83.2%
- 📊 Absolute difference: +7.1 percentage points
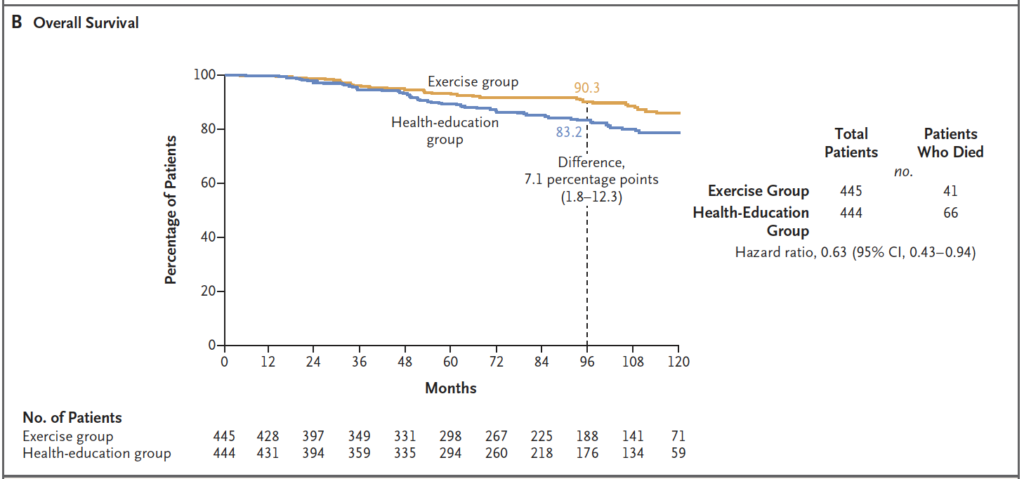
Overall Survival
This represents a magnitude of benefit comparable to many standard approved cancer therapies — from a non-pharmacologic intervention.
🧬 Proposed Mechanisms
Exercise may impact cancer outcomes through multiple biological pathways:
- 🔬 Reduced systemic inflammation
- 🧠 Improved immune surveillance
- 💉 Modulation of insulin and IGF-1
- 🧫 Suppression of micrometastases
- 🧘♂️ Enhanced mitochondrial and metabolic function
💡 Impact on Recurrence and New Primary Cancers
The DFS improvement was largely driven by:
- 🔻 Lower liver recurrence: 3.6% vs. 6.5%
- 🔻 Fewer new primary cancers: 5.2% vs. 9.7%
- Breast cancer: 0.4% vs. 2.7%
- Prostate cancer: 1.1% vs. 2.0%
- Colorectal cancer: 0% vs. 1.1%
💬 Quality of Life and Functional Gains
The exercise group also reported:
- 📈 Sustained improvements in SF-36 physical functioning
- 🚶♀️ Greater gains in 6-minute walk test and VO₂ max
In other words: not only longer life, but better life.
⚠️ Safety Profile
- Musculoskeletal adverse events: 18.5% (exercise) vs. 11.5% (control)
- Grade ≥3 AEs: 15.4% (exercise) vs. 9.1% (control)
💡 These events were expected and manageable with personalized exercise prescriptions.
🔎 Limitations
- 15-year recruitment period
- Fewer-than-expected events (224/380), requiring recalibration of statistical power
- Possible selection bias: healthier patients more likely to enroll
- Greater social interaction in the exercise group may have influenced outcomes
🚀 Conclusions
The CHALLENGE Trial provides Level 1 evidence that a structured exercise intervention:
✅ Improves disease-free survival
✅ Reduces mortality
✅ Enhances functional recovery and well-being
“If exercise were a pill, it would be prescribed in every guideline.”
🩺 Clinical Implications
Integrating exercise into colon cancer care demands:
- Individualized prescription and follow-up
- Behavioral support programs
- Engagement from the multidisciplinary oncology team
📬 Stay Informed. Stay Ahead.
Join the P.life Papers Newsletter and receive the latest evidence-based insights, curated research, and clinical updates on peritoneal oncology — straight to your inbox.
👉 Subscribe now and never miss a breakthrough.
🎧 Listen to the Podcast Episode
Want to dive deeper into this topic?
🎙️ Listen to the full PeritoneoCast episode on Spotify
🧠 This episode was 100% generated using LLM notebook technology and reviewed by the scientific board of Peritoneo.life to ensure clinical accuracy and scientific integrity.
✍️ Dr. Artur Reis
Surgeon | Founder of Peritoneo.life
Portuguese Version
🧬 Exercício e Sobrevivência no Câncer de Cólon: O Ensaio CHALLENGE e Suas Implicações na Prática Oncológica
📍 P.life Papers | Julho 2025
🎙️ Baseado no podcast “Exercício como Tratamento”
📚 Fonte: NEJM, Courneya et al., 2025 – DOI: 10.1056/NEJMoa2502760
Introdução
O câncer colorretal é um dos maiores desafios da oncologia moderna, ocupando o 3º lugar em incidência global e o 2º em mortalidade. Apesar dos avanços no tratamento cirúrgico e quimioterápico, muitos pacientes ainda enfrentam risco significativo de recorrência — especialmente após o tratamento de tumores de cólon em estágio III ou II de alto risco.
Mas e se uma ferramenta simples, acessível e de baixo custo pudesse melhorar significativamente os desfechos desses pacientes?
Foi exatamente isso que o ensaio clínico CHALLENGE investigou — e os resultados surpreendem.
🎯 Objetivo do Estudo
O CHALLENGE Trial foi um estudo randomizado de fase 3 que avaliou se um programa estruturado de exercício físico por 3 anos, iniciado logo após a quimioterapia adjuvante, poderia melhorar a sobrevida livre de doença (SLD) em pacientes com câncer de cólon ressecado.
🧪 Metodologia
- População: 889 pacientes com câncer de cólon (estágio III ou II de alto risco), randomizados 1:1 após completarem a quimioterapia.
- Grupos:
- Grupo Exercício: Suporte comportamental + metas de ≥10 MET-horas/semana.
- Grupo Controle: Apenas materiais de educação em saúde.
- Período de Intervenção: 3 anos.
- Tempo de Seguimento: Mediana de 7,9 anos.
- Desfecho primário: Sobrevida livre de doença (SLD).
- Desfecho secundário: Sobrevida global (SG), função física (objetiva e autorreferida).
📈 Principais Resultados
✅ Sobrevida Livre de Doença (SLD)
- HR: 0,72 (IC 95%: 0,55–0,94; p = 0,02)
- 5 anos:
- Grupo Exercício: 80,3%
- Grupo Controle: 73,9%
- 📊 Diferença: +6,4 p.p.
As curvas de SLD começaram a se separar após 1 ano — com manutenção do benefício por 10 anos.
✅ Sobrevida Global (SG)
- HR: 0,63 (IC 95%: 0,43–0,94)
- 8 anos:
- Grupo Exercício: 90,3%
- Grupo Controle: 83,2%
- 📊 Diferença: +7,1 p.p.
O impacto em SG foi comparável ao de muitas terapias aprovadas hoje — e com uma intervenção não farmacológica.
🧬 Mecanismos Propostos
O benefício clínico pode estar relacionado a múltiplos mecanismos biológicos:
- 💢 Redução da inflamação sistêmica
- 🧫 Melhora da vigilância imune
- 💉 Modulação de fatores de crescimento como insulina e IGF-1
- 🧪 Efeito antiproliferativo em micrometástases hepáticas
- 🧘♂️ Aumento da aptidão física e função mitocondrial
🧠 Impacto Clínico: Recorrência e Novos Tumores
A diferença em SLD foi atribuída principalmente a:
- 🔻 Redução da recorrência hepática: 3,6% vs. 6,5%
- 🔻 Redução de novos cânceres primários: 5,2% vs. 9,7%
- Câncer de mama: 0,4% vs. 2,7%
- Próstata: 1,1% vs. 2,0%
- Colorretal: 0% vs. 1,1%
💬 Função Física e Qualidade de Vida
Pacientes do grupo exercício apresentaram:
- 📈 Melhora sustentada na subescala de função física do SF-36
- 📏 Aumento na distância de caminhada (6MWT) e VO2 previsto
Ou seja, não só sobreviveram mais — como viveram melhor.
⚠️ Eventos Adversos
- Efeitos musculoesqueléticos: 18,5% (grupo exercício) vs. 11,5% (controle)
- Eventos grau ≥3: 15,4% vs. 9,1%
💡 Nenhum sinal de segurança inesperado. O risco foi considerado manejável e proporcional ao benefício.
🔎 Limitações
- Recrutamento lento ao longo de 15 anos
- Número de eventos abaixo do planejado (224/380)
- Possível viés de seleção (pacientes mais saudáveis)
- Maior contato social no grupo exercício pode ter influenciado resultados
🚀 Conclusões e Aplicações
O CHALLENGE Trial fornece evidência de nível 1 de que um programa estruturado de exercício físico iniciado precocemente:
✅ Melhora a sobrevida livre de doença
✅ Prolonga a sobrevida global
✅ Melhora a função física e o bem-estar geral
“Se exercício fosse um comprimido, seria prescrito em todas as diretrizes.”
📌 Implicações para o Futuro
📣 A incorporação do exercício como ferramenta terapêutica deve ser considerada parte integrante do tratamento oncológico adjuvante, exigindo:
- Estrutura de prescrição personalizada
- Programas de suporte comportamental
- Educação multiprofissional e envolvimento do oncologista
📚 Referência Principal
Courneya, K.S. et al. Structured Exercise after Adjuvant Chemotherapy for Colon Cancer. N Engl J Med. 2025. DOI: 10.1056/NEJMoa2502760
📥 Quer receber os próximos artigos diretamente no seu e-mail?
Cadastre-se no P.life Papers Newsletter

